¿En qué consiste la edición genética?
La edición genética permite realizar cambios precisos en el genoma de los organismos. Esto significa hacer modificaciones de manera precisa añadiendo, cambiando o eliminando pares de bases nitrogenadas de la secuencia del ADN. De entre todas las técnicas disponibles, la tecnología CRISPR-Cas9 ha ganado gran popularidad debido a su alta eficiencia, precisión y relativa simplicidad de uso.
¿Cómo funciona CRISPR-Cas9?
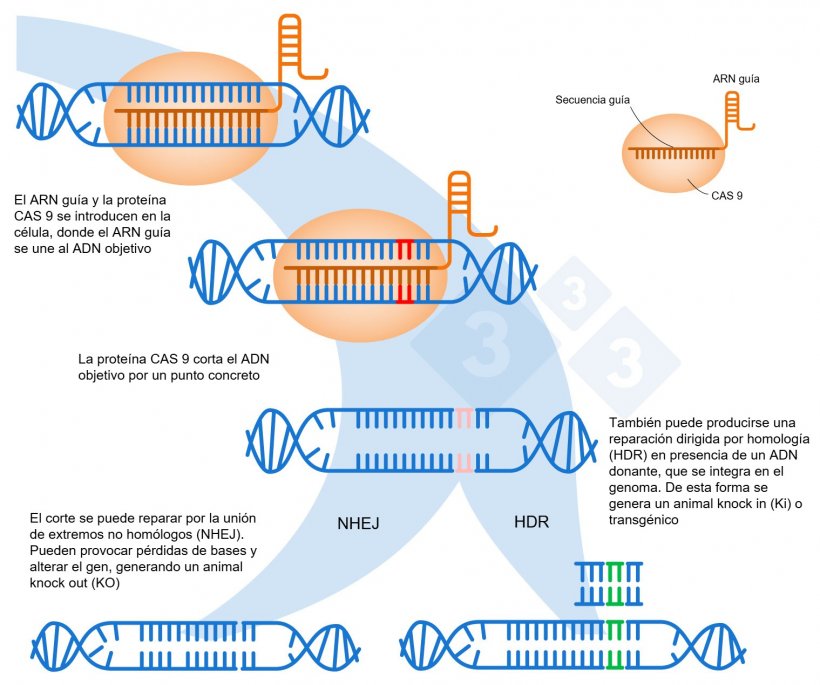
- Se utiliza una guía de ARN, que es una pequeña secuencia de 20 pares de bases que coincide con la parte del ADN que se quiere modificar
- Esta guía lleva a la enzima Cas9 exactamente al lugar donde se debe hacer el corte en las dos cadenas de ADN (Figura 1).
- Tras el corte, el organismo intenta reparar el ADN mediante un proceso llamado unión de extremos no homólogos (NHEJ, por sus siglas en inglés). Durante esta reparación, es posible que se añadan o pierdan algunos pares de bases en el sitio del corte.
- Estos cambios en el ADN pueden alterar el marco de lectura del gen, lo que provoca cambios en la secuencia de aminoácidos de la proteína que ese gen produce. Como resultado, la proteína puede quedar defectuosa o dejar de funcionar por completo (Figura 2).
|
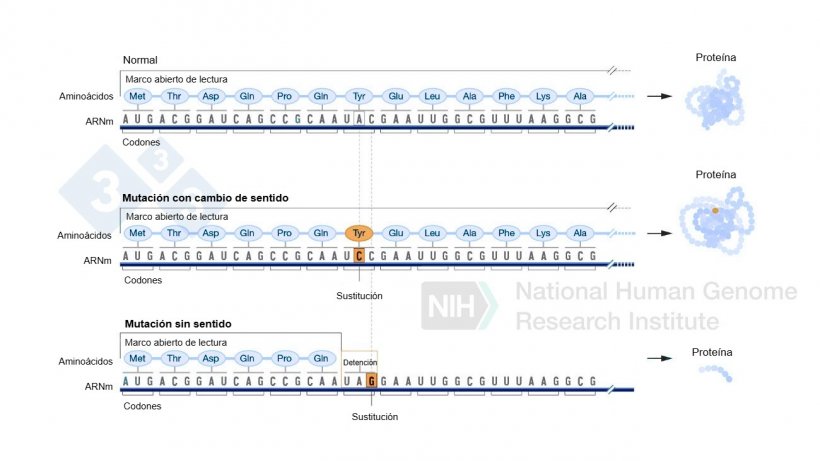
Recordemos que las proteínas están compuestas por largas cadenas de aminoácidos, que son las unidades básicas de las proteínas. Hay 20 tipos diferentes de aminoácidos, y cada uno de ellos está codificado por una secuencia específica de tres bases nitrogenadas en el ADN, conocidas como tripletes o codones. Estas bases pueden ser adenina, citosina, timina y guanina.  Cuando se altera el marco de lectura del ADN (es decir, la forma en que las bases se agrupan en tripletes), la secuencia de codones también cambia. Esto puede dar lugar a la incorporación de aminoácidos incorrectos durante la síntesis de la proteína, o incluso causar la aparición de un codón de parada, lo que interrumpe la formación de la proteína. (Figura 2). |

Animales knock-out: cuando los cambios en el ADN inhabilitan una proteína
Un animal es considerado knock-out (KO) para un gen específico cuando los cambios genéticos desactivan la función de una proteína. Estos cambios son similares a las mutaciones que podrían ocurrir de manera natural a través de procesos espontáneos, pero en este caso, se realizan de manera controlada y dirigida. Por ello, no es posible distinguir si una mutación en un animal ocurrió de forma natural o fue inducida en el laboratorio.
| Es importante destacar que, en este proceso, NO se introduce material genético de otras especies, por lo que los animales KO generados por esta técnica no se consideran transgénicos. |
Un ejemplo de animal KO son los animales resistentes al virus del PRRS. Para que el vPPRS pueda infectar al cerdo, necesita unirse a un receptor específico presente en los macrófagos alveolares de los pulmones del cerdo. Este receptor está codificado por el dominio SRCR5 del gen CD163 (Figura 3). Si este receptor es modificado o eliminado mediante edición genética, el virus ya no puede adherirse a las células, impidiendo la infección y haciendo que el cerdo sea completamente resistente al PRRSv. Esta resistencia genética puede ser heredada por la descendencia, garantizando que las futuras generaciones serán resistentes al PRRS.
Animales Knock-in: Introduciendo nuevas cadenas de ADN y nuevos genes
Una alternativa en la edición genética consiste en aprovechar el momento en que se corta el ADN por Cas9 para introducir una nueva cadena de ADN. Al hacerlo, la célula puede incorporar este nuevo material genético mediante un proceso llamado recombinación homóloga dirigida (HDR, por sus siglas en inglés. Figura 1). Esto permite reemplazar una secuencia de ADN defectuosa por una funcional y corregir el gen para que vuelva a ser operativo o alterar el marco de lectura para generar un animal KO, en el que un gen ha sido desactivado. Además, esta técnica permite insertar un nuevo gen adicional que no tenía antes, en el genoma del organismo, lo que se conoce como knock-in (KI) o transgénico.
| Si el gen que se introduce proviene de otra especie, se crea una combinación genética que no se da de manera natural. A este tipo de organismo se le llama animal transgénico, ya que tiene genes de otra especie integrados en su ADN. |
Un ejemplo de cerdos transgénicos sería aquellos a los que se le ha insertado el gen UPC1, que de manera natural no está en esta especie. Este gen les permite regular mejor su temperatura corporal, lo que los hace más adaptados a soportar bajas temperaturas. Como resultado, los cerdos acumulan menos grasa subcutánea para mantener su temperatura corporal, lo que incrementa el porcentaje de tejido magro (Figura 3).

Editores de bases: una herramienta precisa en la edición genética
Una alternativa más reciente en la edición genética es el uso de los editores de bases, que son enzimas especializadas que, en lugar de cortar el ADN, intercambian de manera precisa un par de bases en una ubicación específica del genoma. Este proceso permite realizar cambios puntuales en el ADN sin generar roturas.
Este tipo de sustitución puede tener varios efectos. En algunos casos, el cambio introduce un codón de parada, lo que detiene la producción de la proteína antes de tiempo, dejándola incompleta y posiblemente no funcional. En otros casos, el cambio altera un aminoácido en la proteína (conocido como una mutación con cambio de sentido), lo que puede modificar su estructura y afectar su función. En ambos casos, estas alteraciones pueden comprometer la funcionalidad de la proteína.
¿Son iguales todos los cerdos editados genéticamente? Regulación Normativa vs. Desarrollo técnico
Es importante entender técnicamente los distintos tipos de edición genética, ya que las regulaciones que se aplican, o deberían aplicarse, varían en cada caso. Actualmente, la mayoría de las legislaciones del mundo limitan estrictamente el uso de animales transgénicos y la comercialización de sus productos. Sin embargo, se está avanzando en la distinción entre animales editados genéticamente y animales transgénicos, lo que podría derivar en regulaciones diferenciadas. Técnicamente, estos dos tipos de modificaciones genéticas son totalmente distintos.
En la Unión Europea, ya se están revisando las normativas referentes a los productos vegetales editados genéticamente, que se denominan nuevas técnicas genómicas (NGT). Esto podría permitir que estas plantas queden exentas de las leyes que regulan a los transgénicos denominados organismos genéticamente modificados (OGM). Sin embrago, hasta la fecha, los animales editados genéticamente siguen estando sujetos a la legislación sobre OMG, lo que limita su desarrollo y futura comercialización.

Proyecto financiado por Fundación Séneca 22065/PI/22.


